Menu Lycée Collège Et Plus
|
Pression et température
I. Mouvement Brownien et chaos moléculaire
……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………...
II. Force pressante exercée par un gaz : 1. Manipulation 1
On utilise une canette que l’on remplie avec très peu d’eau. On pose la canette sur une plaque chauffante, afin de porter l’eau à ébullition. Une fois que l’eau de la canette s’est évaporée, on la retourne au dessus d’un cristallisoir rempli d’eau.
…………………...…………………………………………………………………………………………………………
……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………... ……………………………………………………………………………………………………………………………...
2. Manipulation 2
On utilise une pompe à vide avec sa cloche. Deux ballons fermés contenant un peu d’air sont mis sous la cloche à vide. On actionne la pompe.
…………………………………………………………………………...…………………………………………………
…………………………………………………………………………………………………………………...………… …………………………………………………………………………………………………………………...………… …………………………………………………………………………………………………………………...………… …………………………………………………………………………………………………………………...…………
3. Relation entre force pressante et pression Soit un gaz exerçant une force pressante de valeur F sur une portion de paroi d’aire S. La pression exercée par le gaz est alors définie par le rapport :
L’unité de pression du système international est le Pascal (Pa) mais il existe deux autres unités :
III. Existence de deux échelles de températures : La température est la grandeur qui rend compte de l’agitation thermique des molécules. Plus la température d’un gaz est grande, plus l’agitation des molécules (vitesse de déplacement) est importante.
1. L’échelle Celsius La température est généralement notée θ, l’unité étant le degré Celsius (°C). Cette échelle a été établie à partir des changements d’états de l’eau :
2. L’échelle Kelvin La température absolue est notée T, l’unité étant le Kelvin (K). Cette échelle a été établie an partant du fait qu’à température nulle, l’agitation des molécules devait être nulle. Cette température de 0 K n’est que théorique, les scientifiques ne l’ont pas encore atteinte. La relation entre l’échelle Celsius et l’échelle Kelvin est donnée par : 0 K = -273.15 °C
3. Température et chaleur è Expérience des trois cristallisoirs : eau chaude, eau tiède et eau froide. è Conclusion : ……………………………………………………………………………...……………………………………………… ……………………………………………………………………………...……………………………………………… ……………………………………………………………………………...………………………………………………
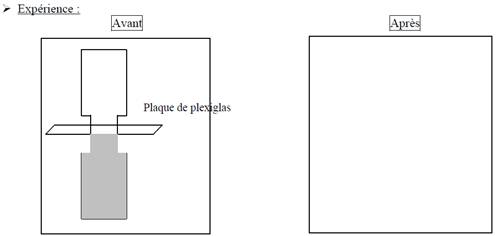
IV. Liens entre pression et température : 1. Lien entre pression et température de changements d’état : expérience du bouillant de Franklin è Expérience : ETAPE 1 : On fait bouillir un peu d’eau dans un erlenmeyer. ETAPE 2 : On bouche l’erlenmeyer. ETAPE 3 : On retourne l’erlenmeyer puis on fait couler un filet d’eau froide sur le fond de l’erlenmeyer.
è Observations : …………………………………...………………………………………………………………………………………… …………………………………………………………...………………………………………………………………… è Interprétation : · Lorsque l'eau bout, de l'eau liquide se transforme en ………………………….. ; celle-ci expulse l'air présent initialement dans le récipient. · Lorsqu'on retire du feu, l'ébullition …………………………..…. donc la température de l'eau est ………………………… à 100 °C. · Avec le filet d’eau froide, on refroidit ……………………..……….. qui se condense et redevient donc liquide ; comme le récipient est bouché, la partie contenant la vapeur se vide, ce qui signifie que la pression au dessus de l'eau est …………………………….. · Plus la pression au dessus de l'eau est basse, plus ………………………………………………….………….. diminue ; lorsqu’on a suffisamment fait …………………………..……………… la température d'ébullition de l'eau, ………………………….……… peut reprendre.
è Applications : · Pourquoi ne peut-on pas faire cuire de bonnes pâtes en montagne ? ………………………………………………………………………………………………………………………...…… ………………………………………………………………………………………………………………………...…… ………………………………………………………………………………………………………………………...…… · Pourquoi les aliments cuisent-ils plus vite dans une cocotte minute ? ………………………………………………………………………………………………………………………...…… ………………………………………………………………………………………………………………………...…… ………………………………………………………………………………………………………………………...……
2. Relation entre pression, température et volume è Expérience : On plonge un flacon de verre dans un cristallisoir rempli d’eau (bain-marie). On relève la pression à l’intérieur du flacon, ainsi que la température de l’eau du cristallisoir.
è Exploitation : On trace la courbe représentant P = f(T) avec P en hPa et T en Kelvin. (Ne faites pas des axes débutant à 0, mais choisissez une origine appropriée).
è Questions :
a) Deux des grandeurs macroscopiques décrivant un gaz sont restées constantes lors de cette manipulation. Lesquelles ? ………………………………………………………………………………………………………………………...……
b) Choisissez parmi les propositions ci-dessous une relation qui soit compatible avec vos observations : P x T = a x V V x T = b x P P x V = c x T (a, b et c sont des constantes)
|
|||||||||||||||||||||||||||||||||||||||