|
Télécharger :  |
L’état gazeux
I. Du
macroscopique au microscopique
Echelle macroscopique à Echelle à taille humaine, de l’ordre du
mètre
Echelle microscopique à grandeur de l’ordre du micromètre
è Voir
simulateur Avogadro - Ampère
1. Description d’un gaz à l’échelle microscopique
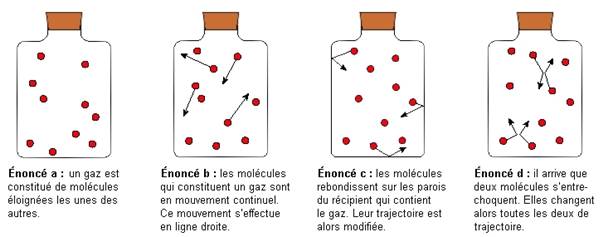
2. Nécessité d’une définition macroscopique
Il est impossible de décrire le mouvement de
chacune des molécules ou de chacun des atomes constituant un gaz.
On décrit un gaz en utilisant les grandeurs
macroscopiques suivantes :
- La température du gaz : elle peut se
mesurer à l’aide d’un thermomètre et s’exprime en Kelvin ou en degré
Celsius.
- Le volume du gaz : c’est le volume
du flacon qui emprisonne le gaz. Il s’exprime en litre (L) ou en mètre
cube (m3) (rem : 1 L = 1 dm3 ou 1 mL = 1cm3).
- La quantité de matière du gaz : elle
s’exprime en mole.
- La pression du gaz : elle s’exprime
en pascal (Pa) (voir paragraphe suivant).
II. Notion de
pression
1. Force pressante
Un gaz exerce une force pressante sur les parois
du récipient qui le contient. Cette force est toujours perpendiculaire à la
paroi.
Si S est la surface sur laquelle un gaz exerce
une force pressante F, la pression P du gaz est donnée par :
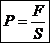
Avec P en pascal (Pa), F en newton (N) et S en
m².
è Ex
10 p 286
L’unité de la pression est le pascal (Pa). On
utilise aussi souvent le bar : 1 bar = 105 Pa. |
|
La pression atmosphérique est égale à 1,013x105 Pa au niveau de la mer.
è Ex
11 p 286
2. Interprétation de la pression d’un gaz
è Voir
document 3 du poly
Quand on comprime un gaz, le volume disponible
pour ses molécules diminue. Les chocs des molécules sur les parois du
récipient contenant le gaz sont plus fréquents.
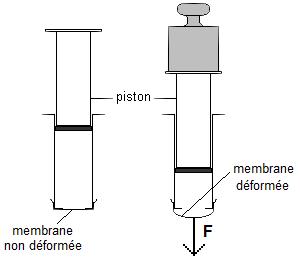
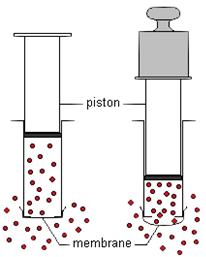
Sur le schéma ci-contre, la membrane se bombe
dans le sens où les chocs moléculaires sont les plus fréquents. Ces chocs sont
d’autant plus fréquents que la pression du gaz est grande.
La forme de la membrane est donc liée à la
pression du gaz à l’intérieur de la seringue et à la pression du gaz à
l’extérieur. La membrane se bombe dans le sens où la force pressante a la
plus grande valeur. |
|
La valeur de la force pressante s’exerçant sur
une surface est égale à la différence des valeurs des forces pressantes
s’exerçant de part et d’autre de la surface.
On mesure la pression avec un manomètre.
III. Notion d’état thermique
Comment réalise-t-on une mesure de
température ?
- On met le thermomètre en contact avec le liquide
le gaz ou le solide dont on veut prendre la température.
- On attend que la température du thermomètre se
stabilise avant de lire la température. C'est-à-dire qu’on attend l’équilibre
thermique.
Définition de l’équilibre thermique : On atteint l’équilibre thermique quand deux corps en contact son à la même
température. Il faut un certain temps pour atteindre cet équilibre.
De nombreux phénomène peuvent renseigner sur
l’état thermique d’un corps :
- La dilatation : le liquide d’un
thermomètre subit une variation de volume en fonction de la température.
- Le rayonnement : tout corps émet un
rayonnement qui dépend de sa température.
- La résistance électrique : la
résistance de certains dipôles électriques varie en fonction de la
température.
è Ex
20 p 287



