|
Télécharger :  |
Spectres
d’émission et d’absorption
1. Réalisation de spectres avec un
prisme
1.1. Spectre de la lumière blanche
But : réaliser un spectre en utilisant un prisme.
Matériel
disponible : lanterne, prisme,
écran
Manipulation : placer entre l’écran et la lampe le prisme et
orientez le de manière à obtenir un spectre sur l’écran |

|
Exploitation :
- Faire un schéma du spectre obtenu.
- Décrire le spectre obtenu en utilisant certains
des termes suivants : continu, raie, bande, émission, absorption (on
pourra s’aider du cours).
- Si l’on approche la main de la lampe, on
s’aperçoit qu’elle est très chaude. En quoi cette observation est-elle en
rapport avec la phrase proposée dans la question 1.
1.2. Etude d’une solution de
permanganate de potassium
But : réaliser le spectre d’une lumière ayant traversée une
solution
Manipulation : On réutilise le montage précédent. On intercale entre
la lampe et le prisme une cuve contenant une solution de permanganate de
potassium.
Exploitation :
- Faire un schéma du spectre obtenu.
- Décrire le spectre obtenu en utilisant certain
des termes suivants : continu, raie, bande, émission, absorption.
- A partir de ce spectre, comment peut-on expliquer
la couleur de la solution ?
2. Visualisation de spectres avec un
spectroscope
Un spectroscope est un dispositif qui permet facilement de décomposer la lumière. Les
spectroscopes que l’on utilise se présentent sous forme de boites en carton. Ils
sont composés d’une fente par laquelle on regarde et d’un réseau qui est un
dispositif qui permet comme le prisme de décomposer la lumière.
2.1. Spectre d’origine thermique
But : Visualiser l’évolution d’un spectre en fonction de la
température de la source.
Observation
: à l’aide d’un spectroscope,
regarder comment évolue le spectre de la lumière émise par une ampoule à
incandescence en fonction de sa tension d’alimentation
Exploitation :
- Comment la température de la lampe évolue-t-elle
lorsque que l’on baisse sa tension d’alimentation ?
- Comment évolue le spectre obtenu quand on diminue
la tension d’alimentation de la lampe ?
- Que peut-on en déduire ?
2.2. Spectre d’une lampe à vapeur de
gaz
Dans une
lampe à vapeur de gaz on excite un gaz par des décharges électriques. Le gaz
émet alors de la lumière.
But : visualiser le spectre d’une lampe à vapeur de gaz
Observation : A l’aide d’un spectroscope, visualiser le spectre
d’une lampe à vapeur de gaz
Exploitation :
- Représenter le spectre observé
- Comment ce spectre est-il appelé ?
- Pourquoi de tels spectres nous renseignent-il sur
la nature du gaz contenu dans l’ampoule de la lampe ?
3. Identification d’espèces chimiques
dans l’atmosphère d’une étoile
But : vérifier la présence de certains éléments dans
l’atmosphère du soleil.
Une
étoile peut être décrite par le schéma ci contre :
Questions :
1. Si on décompose la lumière d’une étoile, quel type
de spectre va-t-on obtenir ?
2. Comment peut-on en déduire la composition de
l’atmosphère d’une étoile ?
|

|
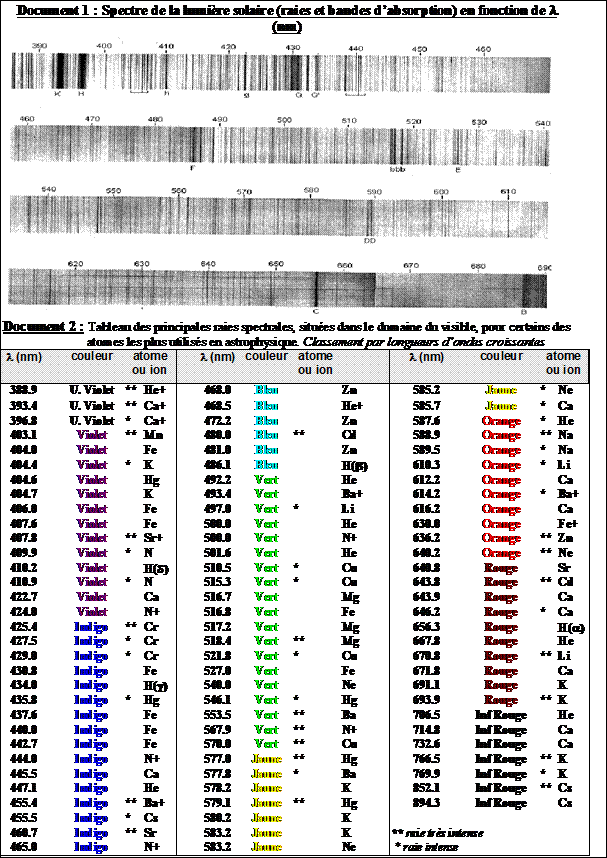
- A partir des deux documents suivants, vérifier que l’atmosphère du Soleil contient les
éléments hydrogène, calcium, magnésium, sodium et fer.
- La bande (B) située à l’extrémité du rouge du
spectre du soleil (document 1) correspond à une absorption par le
dioxygène moléculaire. Y aurait-il du dioxygène à la surface du
Soleil ? Mais comment une telle molécule pourrait-elle exister à
cette température ? Comment peut-on interpréter la présence de cette
bande d’absorption ?