|
Télécharger :  |
Préparation de solutions aqueuses
Le but de ce TP est de déterminer la concentration
d'une solution grâce à sa couleur.
I. Qu’est
ce que la concentration ?
Quelle est la quantité de sel peut-on dissoudre
dans de l'eau ? De permanganate de potassium dans une solution ?
Pour répondre à ces questions, nous ferons appel à
la concentration. C'est la quantité de matière de soluté par unité de volume de
solution. On la note Ccu2+ ou [Cu2+] pour l'ion Cu2+.
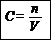
avec C la
concentration molaire en mol.L-1, n en mol et V en L.
1- Calculer
la concentration d'une solution de 500mL contenant 2 moles d'un composé.
2- Calculer
la quantité de matière contenue dans 200 mL d'une solution à 10-1 mol.L-1.
II. La verrerie
utilisée au laboratoire
3- D’après
le document donné ci-dessous, numéroter le matériel donné dans le tableau de
droite.

|
|
Verre de
montre |
|
Pipette
jaugée |
|
Entonnoir |
|
Poire
d’aspiration |
|
Pipette
graduée |
|
Spatule |
|
Agitateur
en verre |
|
Fiole
jaugée |
|
Eprouvette
graduée |
|
Pipeteur |
|
Pissette |
|
Erlenmeyer |
|
Bécher |
|
Burette
graduée |
|
Pipette
simple |
|
Capsule |
Rem :
- Les béchers et les erlenmeyers présentent des graduations peu précises.
On les utilise surtout pour stocker des solutions.
- Les éprouvettes graduées, les fioles jaugées, les pipettes graduées et
jaugées permettent de mesurer des volumes précis.
III. Préparation d'une échelle de couleur
Pour déterminer la concentration d’une solution
inconnue, nous allons préparer une échelle de teinte puis comparer la couleur
de la solution inconnue à celle de ces solutions.
Nous allons réaliser deux échelles de teinte. La
première est réalisée à partir de permanganate de potassium (KMnO4),
la deuxième à partir de sulfate de cuivre (CuSO4). La première étape
est la réalisation d'une solution mère à partir du composé solide puis des
solutions filles à partir de la solution mère.
4- A
l’aide de la fiche pratique, calculer la quantité de solide à prélever pour
réaliser 100mL de la solution mère.
5- Réaliser
la solution mère. --- Appeler le professeur pour l’évaluation ---
6- A
l’aide de la fiche pratique, réaliser les calculs nécessaires à la préparation
de 50mL de la solution fille. La concentration de la solution correspond au
numéro que vous a donné le professeur.
7- Réaliser
la solution fille. --- Appeler le professeur pour l’évaluation ---
8- Quelle
est la fourchette de concentration de la solution inconnue ?
9- Jeter
les solutions à l’évier et nettoyer la paillasse. --- Appeler le professeur
pour l’évaluation ---
Concentrations
en mol.L-1 |
Solution
mère |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
[KMnO4] |
1,0x10-2 |
2,0x10-3 |
1,0x10-3 |
6,0x10-4 |
4,0x10-4 |
2,0x10-4 |
1,0x10-4 |
6,0x10-5 |
4,0x10-5 |
[CuSO4] |
2,0x10-2 |
4,0x10-3 |
2,0x10-3 |
1,6x10-3 |
1,2x10-3 |
8,0x10-4 |
4,0x10-4 |
2,0x10-4 |
1,2x10-4 |
Fiches pratiques |
Réalisation
d'une solution mère à partir d'un composé solide.
1- Calcul
de la quantité de matière à partir de la concentration : si vous
souhaitez avoir un volume V de solution à la concentration C, calculer le
nombre de mole par la formule n = C x V.
2- Calcul
de la masse molaire : calculer la masse molaire du composé à peser
(penser à regarder la formule ou la masse molaire sur le flacon).
3- Calcul
de la masse de solide à peser : Vous souhaitez alors obtenir n mole
de ce composé, calculez la masse à peser à partir de la formule m = n x M.
4- Peser
cette masse dans une coupelle souple en plastique (utiliser une spatule pour
prélever le solide).
5- Verser
le solide dans une fiole jaugée du volume désiré.
6- Rincer
la coupelle avec de l'eau distillée au dessus de la fiole. Attention à
entrainer tous les grains de matière dans la fiole.
7- Remplir
à moitié la fiole jaugée, agiter cette fiole sans la retourner (il ne
faut pas de liquide au dessus du trait de jauge).
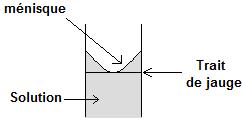
8- Compléter
la fiole jaugée jusqu'au trait de jauge comme le montre le schéma
suivant :
|
Réalisation
d'une solution fille à partir d'une solution mère.
1- Calculer
la quantité de matière dans la solution finale : si vous souhaitez
avoir un volume V de solution fille à la concentration C, calculer le nombre
de mole par la formule n = Cfille x Vfille.
2- Calcul
du volume de solution mère à prélever : vous souhaiter alors
prélever cette quantité de matière dans la solution mère. Calculez le volume
de solution mère à prélever grâce à la formule Vmère = ndésiré / Cmère.
3- Mesurer
ce volume à l'aide d'une pipette jaugée ou à défaut d'une pipette graduée.
Important : ne pas prélever la solution mère directement dans la fiole
jaugée, utiliser un bécher.
4- Verser
ce liquide dans une fiole jaugé du volume désiré.
5- Remplir
à moitié la fiole jaugée, agiter cette fiole sans la retourner (il ne
faut pas de liquide au dessus du trait de jauge).
6- Compléter
avec de l'eau distillée jusqu'au trait de jauge.
|
IV. Grille d’évaluation |
Pesée du solide |
X
X |
Dissolution du solide |
X
X |
Prélèvement de la solution mère |
X
X |
Dilution de la solution |
X
X |
Rangement de la paillasse |
X
X |
Note finale |
/ 10 |
|


