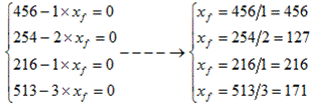Menu Lycée Collège Et Plus
|
Transformation chimique d’un système
Définition d’un système chimique : C’est un mélange d’espèces chimiques. Pour le décrire, on a besoin de connaitre sa pression, sa température, le nom ou la formule des espèces chimiques le constituant, leur quantité de matière et leur état physique (solide, liquide ou gazeux).
I. La transformation chimique
Qu’avons-nous fait dans le TP de chimie n°13 ?
· Description de l’état initial d’un des systèmes chimiques étudiés : ü V = 150 mL de vinaigre (acide éthanoïque, formule brute : CH3COOH, aqueux) ü m = 9,0 g de bicarbonate de sodium (hydrogénocarbonate de sodium, formule brute : NaHCO3, solide) ü (T "H 20°C, P "H 1 bar) · Description de l’état final correspondant (les quantités de matières sont inconnues): ü Dioxyde de carbone : CO2 (gazeux) ü Acétate de sodium : CH3COONa (aqueux) ü Eau : H20 (liquide) ü Bicarbonate de sodium ü (T "H 20°C, P "H 1 bar)
Rem : A la fin de la transformation chimique, on a remarqué le bicarbonate de sodium avait totalement disparu.
Définition de la transformation chimique : Il y a transformation chimique lorsqu’une nouvelle espèce chimique apparait dans le système et lorsqu’une des espèces introduites initialement disparaît.
Rem : La transformation chimique s’arrête quand l’une des espèces présentes initialement a totalement disparu.
è Ex 8 et 12 p 148
II. Modélisation par le chimiste de la transformation : la réaction chimique
è Définition de modélisation à rappeler à l’oral
La description de la transformation d’un système chimique est généralement complexe. Nous allons la modéliser par la réaction chimique qui ne s’intéresse qu’à la transformation des réactifs et à la formation des produits.
Définition de la réaction chimique : la réaction chimique permet d’indiquer dans quelles proportions les réactifs sont consommés et les produits sont formés. Elle indique aussi leur état physique.
On la symbolise par une équation : Réactif 1 + Réactif 2 + … à Produit 1 + Produit 2 + … Le sens de la flèche indique le sens dans lequel le système chimique évolue.
Exemples :
(s) : solide, (l) : liquide, (g) : gazeux et (aq) : aqueux (en solution dans de l’eau)
Rem :
- Conservation des éléments chimiques de part et d’autre de la flèche. - Conservation de la charge électrique globale de part et d’autre de la flèche : charge des réactifs = charge des produits.
Exercice d’application : ajustement d’une équation chimique On considère la transformation chimique qui permet de produire de l’éthanol (C2H6O) et du dioxyde de carbone (CO2) à partir de glucose (C6H12O6). Cette transformation chimique peut être modélisée par la réaction chimique suivante : C6H12O6 (s) à C2H6O (l) + CO2 (g) 1- Compter les éléments constituant les réactifs et les éléments chimiques constituant les produits. 2- L’équation donnée respecte-t-elle la règle de conservation des éléments chimiques ? 3- Ajuster les coefficients stœchiométriques de l’équation pour respecter cette règle et donner l’équation chimique correcte.
On considère la réaction entre les ions fer III et le zinc symbolisée par l’équation chimique suivante : Fe3+ (aq) + Zn (s) à Fe (s) + Zn2+ (aq) 4- Donner la charge électrique globale des réactifs ainsi que celle des produits. 5- L’équation donnée respecte-t-elle la règle de conservation de la charge électrique globale ? 6- Ajuster les coefficients stœchiométriques de l’équation pour respecter cette règle et donner l’équation chimique correcte.
è Ex 15 p 149
III. Bilan de matière
Un bilan de matière consiste à déterminer la composition d’un système chimique au cours d’une transformation chimique (quantité de réactifs disparue, quantité de produits apparue).
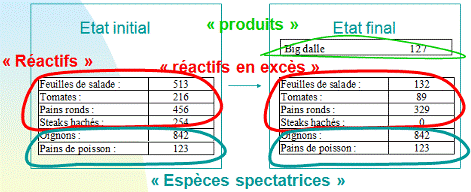
è Voir activité Big Dalle Tableau d’avancement
Cherchons quel ingrédient va disparaitre en premier :
è Application à la chimie : retour sur le TP n°13 (ballons) L’expérience du prof : mélange de 3,0g de bicarbonate de sodium (NaHCO3) et de 50 mL de vinaigre (5,0.10-2 mol de CH3COOH). On a : M(NaHCO3) = MNa + MH + MC + 3 x MO = 23,0 + 1,0 + 12,0 + 3 x 16,0 = 84 g.mol-1. Donc n(NaHCO3) = m(NaHCO3) / M(NaHCO3) = 3,0 / 84 = 3,6.10-2 mol.
On cherche à calculer l’avancement dans l’état final (xmax). On cherche quel est le réactif limitant (celui qui va disparaître en premier) :
Donc dans l’état final du système chimique sera le suivant : è 5,0.10-2 - 3,6.10-2 = 1,4.10-2 mol de vinaigre è 3,6.10-2 mol d’acétate de sodium è 3,6.10-2 mol de dioxyde de carbone è Excès d’eau
Définition de l’avancement d’une réaction chimique : C’est une valeur variable notée x, qui permet de déterminer les quantités de matière de réactifs transformés et de produits formés.
Rem :
Définition du réactif limitant : A l’état final, la quantité de matière de ce réactif est nulle. Rem : les autres réactifs, dont la quantité de matière n’est pas nulle a l’état final, sont dit en excès.
è Ex 10 p 162, ex 15 p 163
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||