Menu Lycée Collège Et Plus
|
Outils de description d’un système
I. La mole : unité de quantité de matière 1. La mole
Définition quantité de matière : C’est un nombre d’entités chimiques, c'est-à-dire un nombre d’atomes, d’ions ou de molécules identiques.
Définition de la mole : La mole est l’unité de quantité de matière utilisée par les chimistes. Une mole d’atomes contient 6,022.1023 atomes.
Rem : Le nombre 6,022.1023 est appelé nombre d’Avogadro. On le note NA.
Exemple : Combien de particules sont contenues dans n = 3,0 mol d’eau ? On a N = n x NA = 3,0 x 6,022.1023 = 1,8.1024 !! Soit 1,8 millions de milliards de milliards d’atome !!
2. Masse molaire atomique
Définition de la masse molaire atomique : La masse molaire d’un élément chimique est la masse d’une mole de cet élément chimique. Elle s’exprime en gramme par mole (g.mol-1).
Exemple : Déterminer la masse molaire du sodium (A = 23). Pour un atome de chlore, on a : mNa = A x mnucléon = 23 x 1,67.10-27 = 3,84.10-26 kg. La masse molaire de l’atome est donc égale à : M(Na) = mNa x NA = 3,84.10-26 x 6,022.1023 = 0,0231 kg.mol-1 = 23,1 g.mol-1.
Rem : - Les masses molaires des atomes figurent dans la classification périodique des éléments. - La masse molaire d’un ion est égale à celle de l’atome correspondant.
3. Masse molaire moléculaire
1) D’après le document, la masse de 6,81.10-3 mol d’urée est de 0,41g. Donc M(urée) = 0,41 / 6,81.10-3 = 60 g.mol-1. 2) La somme des masses molaires des atome de l’urée est : M(C) + 4 x M(H) + 2 x M(N) + M(O) soit 12 + 4 x 1 + 2 x 14 + 18 = 60 g.mol-1. 3) On constate que la masse molaire moléculaire est égale à la somme des masses molaires de chaque atome constituant la molécule. 4) M(cholesterol) = 2,29 / 5,93.10-3 = 386 g.mol-1. 27 x M(C) + 46 x M(H) + M(O) = 27 x 12 + 46 x 1 + 16 = 386 g.mol-1. On retrouve bien le résultat de la question 3). 5) On a n = m / M(cholesterol) = 9,0 / 386 = 0,023 mol.
Définition de la masse molaire moléculaire : La masse molaire moléculaire est égale à la somme des masses molaires de chaque atome constituant la molécule.
4. Calcul d’une quantité de matière La quantité de matière n d’une masse m d’un échantillon de masse molaire M est donnée par la relation :
(n en mol, m en g et M en g.mol-1)
5. Le volume molaire
Définition du volume molaire : Le volume molaire d’une espèce chimique est le volume occupé par une mole de cette espèce.
II. Concentration molaire 1. Dissolution d’une espèce chimique
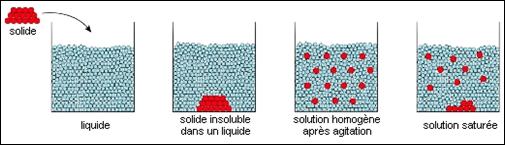
Exemple :
Représentation microscopique de l’introduction d’un solide moléculaire dans un liquide
2. Concentration molaire
è Voir TP de chimie n°12
Définition de la concentration molaire : C'est la quantité de matière de soluté par unité de volume de solution. On la note Ccu2+ ou [Cu2+] pour l'ion Cu2+.
avec C la concentration molaire en mol.L-1, n en mol et V en L.
è Ex 9 p 134 et 15 p 135
3. Dissolution d’un solide, dilution d’une solution
è Voir TP de chimie n°12
Los d’une dilution, la concentration molaire de soluté diminue, mais sa quantité de matière ne change pas.
è Ex 19 p 135
|
|||||||||