Menu Lycée Collège Et Plus
|
Représentation de Lewis des molécules Objectifs :
I. Rappels 1. Qu’est-ce qu’une molécule ?
2. Formule brute d’une molécule Les symboles des éléments présents dans la molécule sont écrits côte à côte avec, en indice, en bas à droite, le nombre d’atomes de chaque élément. L’indice 1 n’est jamais spécifié.
Exemple : Le sucre de cuisine est formé de molécules de saccharose de formule brute C12H22O11. Cette formule indique qu’une molécule de saccharose est formée par l’association de ……………………………………………………………. …………………………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………………………… .
II. Formule de Lewis des molécules, règles du duet et de l’octet Comment, dans la molécule de saccharose, les différents atomes sont-ils liés entre eux ? L’application de la règle de l’octet (et du duet) ainsi que l’utilisation de la formule de Lewis permet de répondre à cette question.
1. Règles du duet et de l’octet Les atomes constituant les gaz nobles (hélium, néon, argon,…) sont les seuls atomes qui existent de manière isolée dans la nature. Quelle est leur structure électronique ?
Exemple : 1) Quel est la structure électronique de l’atome d’oxygène (Z = 8) ? ………………………………………………………… 2) Que fait l’atome pour respecter la règle du duet ou de l’octet ? …………………………………………………………… …………………………………………………………………………………………………………………………………………………………………….. 3) Quelle est alors sa structure électronique ? ………………………………………………………………………………………….. 4) Qu’en déduit-on ? ....................................................................................................................................... ………………………………………………………………………………………………………………………………………………………………………
2. Exemple : la molécule de chlorure d’hydrogène Quelle est la formule brut de cette molécule ? ………………………………………. Quelle est la structure électronique des deux atomes la composant ? Hydrogène : Z = 1 à ………………………………………………. Chlore : Z = 17 à …………………………………………………….
III. Méthode de détermination de la représentation de Lewis d’une molécule Écrire le nom et la formule brute de la molécule. ‚ Écrire la structure électronique de chaque atome. ƒ Trouver le nombre ne d’électrons externes de chaque atome. „ Trouver le nombre nl de liaisons covalentes que doit établir l’atome pour acquérir une structure en octet (8–ne) ou en duet (2–ne) suivant la règle à laquelle il est soumis. … Calculer le nombre nnl de doublets non liants de chaque atome : nnl = (ne - nl) / 2
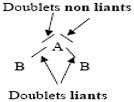
On peut alors dessiner la représentation de Lewis : † Placer le(s) doublet(s) liant(s) entre les atomes de la molécule (liaisons covalentes). ‡ Placer le(s) doublet(s) non liant(s) autour des atomes qui en possèdent ˆ Vérifier que chacun des atomes de la molécule satisfait à la règle de l’octet en étant entouré de 4 doublets (ou d’un seul doublet pour la règle du duet).
IV. Application de la méthode Déterminer la représentation de Lewis des molécules suivantes en complétant le tableau donné puis construire le modèle éclaté de cette molécule à l’aide des boites de modèles moléculaires : Dihydrogène H2 ; Dichlore Cl2 ; Chlorure d’hydrogène HCl ; Méthane CH4 ; Ammoniac NH3 ; Éthane C2H6 ; Dioxygène O2 ; Diazote N2 ; Éthylène C2H4 ; Dioxyde de carbone CO2. Données :
V. Pour les plus rapides Etablir la représentation de Lewis des molécules organiques suivantes : a) Acide cyanhydrique : HCN b) Méthanal : CH2O c) Méthylamine : CH5N d) Méthanol : CH4O e) Perchlo : C2Cl4 |
|||||||||||||||||||||||||||||||||||||||||||||