Menu Lycée Collège Et Plus
|
De l’atome aux édifices chimiques
I. Les gaz nobles
Définition gaz nobles : Ce sont : l’hélium (He, Z =2) ; le néon (Ne, Z = 10) et l’argon (Ar, Z = 18) (+ krypton ; xénon et radon). Les atomes des gaz nobles présentent une grande inertie chimique (ils ne sont impliqués dans aucune transformation chimique).
Dans le TP n°9, on a vu que ces gaz on une structure électronique externe en octet (huit électrons sur la couche externe) sauf pour l’hélium qui a une structure électronique en duet (deux électrons sur la couche externe). Ex : Ne à (K)2 (L)8
Règle du duet et de l’octet : Les atomes qui n’ont pas la structure stable en duet ou en octet captent, cèdent ou mettent en commun des électrons pour l’acquérir.
Rem : Lorsque la structure électronique d’un élément change, son noyau reste intact, seul le nombre d’électrons sur la couche externe est modifié.
II. Les ions monoatomiques
è Voir exemple de l’oxygène dans le TP n°9
Définition ion monoatomique : Les ions monoatomiques sont des atomes dont le nombre d’électrons a été modifié pour satisfaire à la règle de l’octet ou du duet.
Rem : L’application de la règle de l’octet ou du duet permet de prévoir la charge électrique des ions monoatomiques qui peuvent se former.
è Ex 10 p86
III. Représentation de Lewis des molécules 1. Les molécules
è Voir TP n°9
Dans une molécule, les atomes mettent en commun des électrons de leur couche externe. Chacun d’eux s’entoure ainsi des électrons requis pour respecter le règle de l’octet ou du duet.
Définition de la liaison covalente : La mise en commun de deux électrons par deux atomes est une liaison covalente (ou doublet liant). Pour la représenter, on trace un tiret entre les symboles des deux atomes.
Exemple : H-H.
Rem : 1) Dans la molécule, les atomes sont plus stables que s’ils étaient isolés. 2) Les électrons externes d’un atome qui ne sont pas engagés dans une liaison covalente se groupent par paires pour former des doublets non-liants. On les représente par un tiret tracé autour de l’atome concerné.
Définition de la représentation de Lewis : Elle consiste à dessiner le symbole de chacun des atomes présents dans la molécule, ainsi que les positions des doublets liants et non liants.
è Pour déterminer la représentation de Lewis d’un atome voir la méthode dans le paragraphe III du TP n°9.
2. Formule d’une molécule
Formule brute : Les symboles des éléments sont écrits côte à côte avec en indice (en bas à droite) le nombre d’atomes de chaque élément.
Formule développée : On écrit le symbole de tous les atomes ainsi que toutes les liaisons covalentes.
Formule semi-développée : On écrit le symbole de tous les atomes ainsi que toutes les liaisons covalentes sauf les liaisons concernant les atomes d’hydrogène.
Exemple : Ecrire les formules développée et semi-développée de la molécule C4H10.
3. Isomères
Définition : Deux isomères sont deux molécules qui ont la même formule brute mais pas la même formule développée.
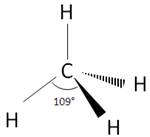
IV. Géométrie des molécules 1. Représentation de CRAM
Pour représenter la géométrie des molécules, on utilise soit des modèles moléculaires comme ceux utilisés lors du TP n°9, ou alors ou utilise la représentation de CRAM :
2. Le modèle de Gillespie
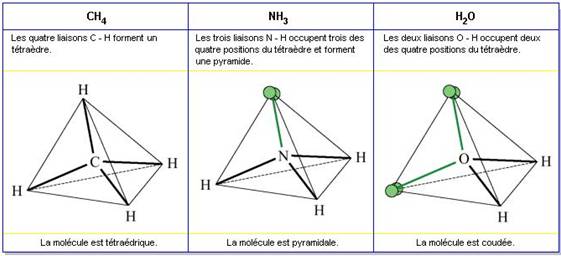
Afin de prévoir la géométrie des molécules, on utilise le modèle de Gillespie.
A cause de leur charge électrique, les doublets d’électrons appartenant à une molécule ont tendance à s’éloigner le plus possible les uns des autres. Les atomes sont disposés dans l’espace de telle manière que les doublets d’électrons soient les plus éloignés possibles.
Exemple :
|
||||||||