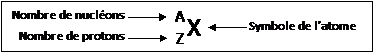Menu Lycée Collège Et Plus
|
Modèle de l’atome è Voir document 1 du polycopié
I. Structure de l’atome Un atome est constitué d’un noyau et d’électrons en mouvement autour du noyau. 1. Le noyau
Définition d’un nucléon : le noyau est constitué de particules appelées nucléons. Ces particules sont de deux types : les protons et les neutrons.
Définition du nombre de charge ou numéro atomique : c’est le nombre de protons du noyau. On le note Z.
Le nombre de nucléons du noyau se note A. Le nombre de neutrons du noyau se note N. On a : A = Z +N.
è Voir document n°2 du polycopié.
2. Les électrons
Un atome est électriquement neutre. Si son noyau contient Z charges positives (protons), l’atome doit contenir Z charges négatives donc Z électrons.
3. Symbole du noyau Les atomes sont symbolisés de la manière suivante :
Exemple : Le noyau de cuivre contient 29 protons et 34 neutrons. Donner son symbole ? Combien d’électrons possède l’atome de cuivre ?
Ex 13 et 14 p70
4. Masse de l’atome
Or me est négligeable devant mp et mp ~ mn donc
Conclusion : La masse d’un atome est essentiellement concentrée dans son noyau car la masse des électrons est négligeable devant celle des nucléons. On a :
Ex 15 p70
II. L’élément chimique
è Voir poly document 3
1. Isotopes Définition isotope : On appelle isotopes des atomes possédant le même nombre de protons et d’électrons mais un nombre de neutrons différent.
Exemple : Il existe trois isotopes du
carbone : le carbone 12 (
2. Les ions
Définition : Un ion monoatomique est formé à partir d’un atome qui a perdu ou gagné des électrons.
Remarque : La structure du noyau n’est pas modifiée, donc l’ion monoatomique possède le même nombre de protons et de neutrons que l’atome correspondant.
Le symbole d’un ion est le symbole de l’atome auquel on ajoute en haut à droite sa charge électrique globale.
Exemple : L’ion cuivre II a pour formule Cu2+, car il possède une charge électrique globale de +2e, ce qui signifie qu’il a perdu deux électrons par rapport à l’atome de cuivre.
Conclusion : Un atome est électriquement neutre, car le nombre d’électrons du nuage électronique est égal au nombre de protons du noyau, tandis que leur charge est opposée. Un cation est un ion positif, car le nombre d’électrons du nuage électronique est inférieur au nombre de protons du noyau. Un anion est un ion négatif, car le nombre d’électrons du nuage électronique est supérieur au nombre de protons du noyau.
3. Caractérisation de l’élément chimique par son numéro atomique
A chaque numéro atomique Z correspond un élément chimique.
Voir exemples sur le document 4 du polycopié.
Conclusion TP n°6 de chimie : Lors d’une transformation chimique, tous les éléments chimiques présents avant la transformation sont nécessairement aussi présents après. On dit qu’il y a conservation des éléments chimiques lors des transformations chimiques.
III. Un modèle du cortège électronique
è Voir poly documents 5 et 6
Les électrons d’un atome sont placés sur différentes couches : · La première couche est appelée couche K. Elle peut contenir au maximum 2 électrons. · La seconde couche est appelée couche L. Elle peut contenir au maximum 8 électrons. · La troisième couche est appelée couche M. Elle peut contenir au maximum 18 électrons · etc.
Répartition des électrons sur chaque couche (pour les atomes tels que Z≤18) :
Rem : La dernière couche occupée s’appelle la couche externe, les autres couches sont les couches internes de l’atome. Définition de la structure électronique d’un atome: C’est la répartition des électrons de cet atome dans les différentes couches électroniques. Elle se note (K)x(L)y(M)z…, où K, L, M, … sont les noms des couches électroniques, et x, y, et z représentent le nombre d’électrons présents dans chaque couche.
Exemple : Le numéro atomique de l’aluminium est Z = 13, donc l’atome d’aluminium contient 13 électrons. Sa structure électronique s’écrira donc : (K)2(L)8(M)3. Il y a 10 électrons sur les couches interne et 3 électrons sur la couche externe.
è Ex 29 p71 |
|||||||||||||||||||||