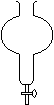Menu Lycée Collège Et Plus
|
TP N°5 : Synthèse d’une espèce chimique Objectifs : - Réaliser la synthèse d’un ester aromatique à forte odeur de banane, l’acétate d’isoamyle ; - Suivre un protocole expérimental en respectant les consignes ; - Connaître le montage du chauffage à reflux.
Les esters sont à l’origine du goût et de l’odeur agréable de nombreux fruits, fleurs et parfums artificiels. Les senteurs naturelles doivent leur délicatesse à des mélanges complexes contenant souvent plus de cent espèces chimiques différentes. Par contre, les parfums artificiels sont souvent constitués d’une seule espèce chimique ou d’un mélange très simple ce qui les rend moins coûteux.
1. La transformation chimique L’acétate d’isoamyle est un ester présent dans certaines plantes (jasmin, eucalyptus, bergamote) et dans la banane. Il est utilisé dans l’alimentation comme arôme de banane, et à faibles doses, en parfumerie. On veut réaliser sa synthèse. 1.1. Les réactifs et les produits
1.2. La transformation chimique L’acide éthanoïque et l’alcool isoamylique réagissent pour donner l’acétate d’isoamyle et de l’eau. Dans cette synthèse, l'acide éthanoïque sera introduit en excès. La transformation chimique est lente. Pour l’accélérer, on chauffe le mélange réactionnel et on ajoute un catalyseur : l’acide sulfurique (l’acide sulfurique est très soluble dans l’eau).
2. Sécurité Les fiches de sécurités associées aux réactifs utilisés sont données ci-dessous :
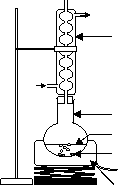
3. Synthèse de l’acétate d’isoamyle 3.1. Protocole expérimental è Dans un ballon contenant déjà 15 mL d’acide éthanoïque et 10 gouttes d’acide sulfurique concentré, introduire avec précaution 10 mL d’alcool isoamylique mesuré à l'éprouvette graduée et quelques grains de pierre ponce. è Placer le ballon dans le chauffe-ballon et le fixer à l’aide d’une pince. è Fermer le ballon à l’aide du réfrigérant à eau. è Relier le réfrigérant au robinet è Faire vérifier votre montage par le professeur ! è Porter à ébullition douce pendant environ 25 min. è Éteindre le chauffe-ballon, baisser le support élévateur et laisser refroidir. 3.2. Principe du chauffage à reflux
4. Extraction de l’acétate d’isoamyle synthétisé. 4.1. Protocole expérimental è D’une manière générale, les espèces chimiques organiques sont moins solubles dans l’eau salée que dans l’eau. Verser le mélange obtenu dans un verre à pied contenant environ 60 mL d’eau salée (solution concentrée de chlorure de sodium) : c’est le relargage. è Verser le contenu du verre à pied dans une ampoule à décanter. Agiter en évacuant le gaz qui se dégage. è Après décantation, récupérer la phase organique dans un petit bécher. 4.2. Extraction de l’espèce synthétisée Pour répondre aux questions suivantes, penser à s’aider du tableau donné dans le paragraphe 1.1.
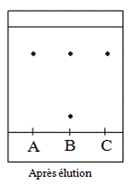
5. Identification de l’espèce synthétisée Après avoir synthétisé une espèce chimique, il faut la caractériser pour être sûr qu’elle correspond bien à l’espèce chimique attendue. Pour cela, à l’aide de l’éluant adéquat, on réalise une C.C.M (chromatographie sur couche mince) avec le produit synthétisé (noté A), l'arôme de banane commercial (noté B) et l’acétate d’isoamyle pur (C). On obtient le chromatogramme ci-contre.
|
|||||||||||||||||||||||||||||||||||||||||||||||||